CINÉTICA ENZIMATICA (ecuación de michaelis Km)
Cinética en Saint Marc: Modelos de Enzimas y Factores que Afectan la Velocidad de Reacción
Resumen de la Sección: En esta sección, se aborda la cinética en Saint Marc, específicamente los modelos de enzimas sustratos (Fisher y Koshland) y los factores que influyen en la velocidad de reacción enzimática.
Modelos de Enzimas Sustratos
- Se mencionan dos modelos de enzima sustrato: el modelo de Fisher y el modelo de Koshland.
- El modelo de Fisher describe una unión perfecta entre sustrato y enzima, como una llave y cerradura. En contraste, el modelo de Koshland es un ajuste inducido donde el sustrato modifica la forma de la enzima para permitir la unión.
Mecanismos de Acción Enzimática
- Las enzimas actúan a través de mecanismos como proximidad, acidobásico y covalente para facilitar las reacciones bioquímicas.
Estudio de Velocidad en Reacciones Enzimáticas
- La cinética enzimática estudia la velocidad y los factores que afectan las reacciones. La concentración del sustrato es fundamental para determinar la velocidad.
- La relación entre concentración del sustrato y velocidad se representa mediante la curva sustrato-velocidad. A mayor sustrato, mayor velocidad hasta alcanzar una velocidad máxima.
Constante Demichelis y Afinidad Enzima-Sustrato
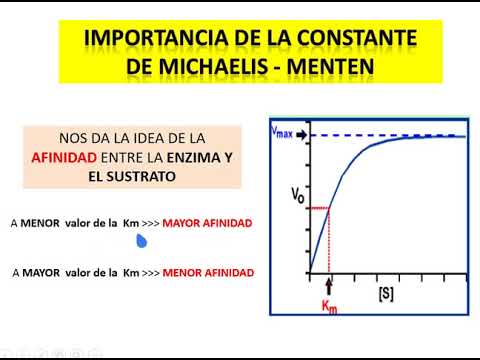
- La constante Demichelis indica la cantidad necesaria de sustrato para alcanzar la mitad de la velocidad máxima. Una alta afinidad entre enzima-sustrato conlleva a una menor constante Demichelis.
- La afinidad entre enzima-sustrato influye directamente en la saturación rápida o lenta de una enzima, impactando así en la constante Demichelis.
Importancia Práctica: Ejemplo del Alcohol
- Se ilustra con un ejemplo práctico sobre cómo diferentes formas (alta o baja afinidad) de una misma enzima pueden influir significativamente durante procesos metabólicos como el metabolismo del alcohol.
Afinidad enzimática y factores que influyen
Resumen de la sección: En esta parte, se discute la importancia de la afinidad enzimática y los factores que influyen en las reacciones enzimáticas.
Afinidad Rápida y Saturación Enzimática
- La constante baja de afinidad rápida conlleva a una saturación enzimática, lo que permite al acetaldehído libre reaccionar y producir vasodilatación.
- El componente no metabolizado produce taquicardia facial al saturarse las enzimas.
Factores que Influyen en las Reacciones Enzimáticas
- La temperatura óptima o elevada aumenta el movimiento del sustrato, incrementando la velocidad de reacción.
- Un pH óptimo de 5.9 mejora la velocidad de reacción.
- El sustrato alcanza su velocidad máxima cuando implementado, afectando directamente la producción de productos.
Curvas de Velocidad y Sustrato
Resumen de la sección: Se analiza cómo varía la velocidad de producción con respecto a la cantidad de sustrato presente.
Relación entre Cantidad de Sustrato y Velocidad
- Aumentar la molécula del sustrato incrementa significativamente la velocidad de producción.
- Sin embargo, al seguir aumentando el sustrato, puede llegar un punto donde la enzima se satura, limitando así el aumento en velocidad.
Factores Externos: Temperatura y pH
Resumen de la sección: Se exploran los efectos de temperatura y pH en las reacciones enzimáticas.
Influencia de Temperatura y pH
- Una temperatura elevada aumenta el movimiento del sustrato pero temperaturas extremas desnaturalizan las proteínas enzimáticas.
- Incrementar el pH favorece ligeramente la reacción; sin embargo, valores extremos desnaturalizan o ralentizan las proteínas.
Inhibición Enzimática: Competitiva vs. No Competitiva
Resumen de la sección: Se detalla cómo ciertos factores pueden inhibir las reacciones enzimáticas, diferenciando entre inhibidores competitivos y no competitivos.
Tipos de Inhibición
- Los inhibidores competitivos compiten con el sustrato por unirse al sitio activo, disminuyendo así la afinidad.