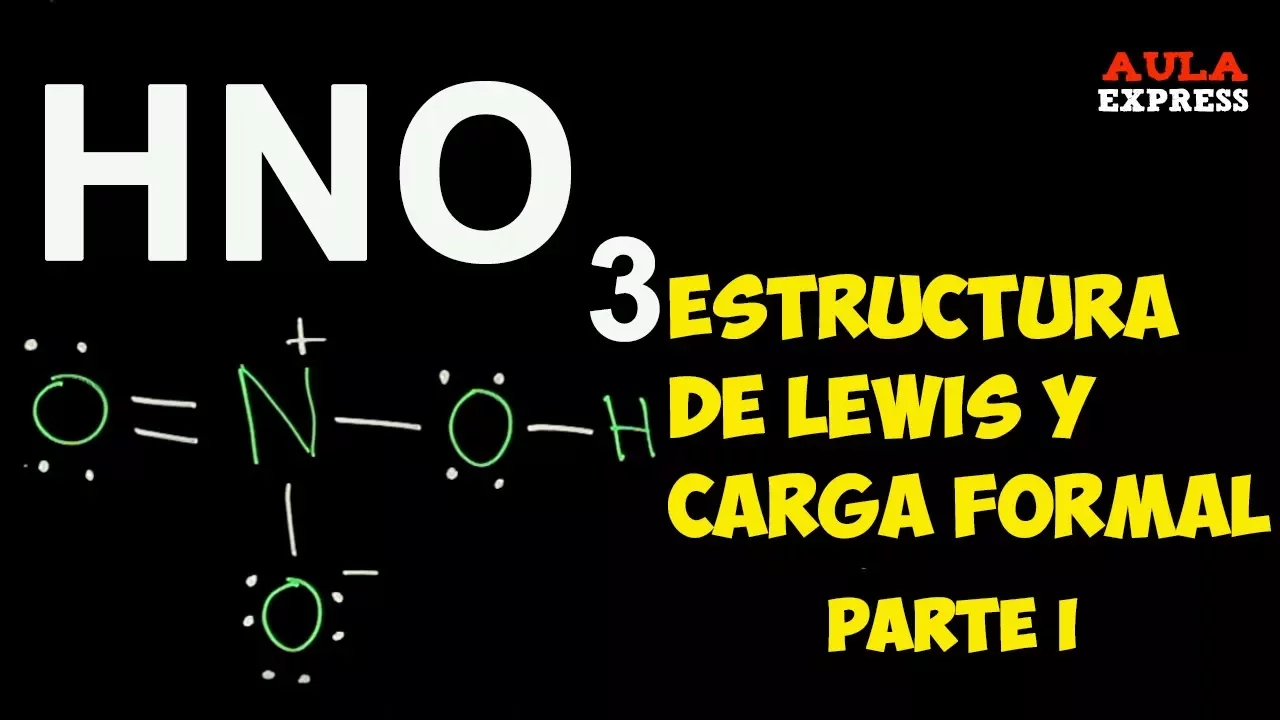
Estructura de Lewis Acido Nítrico HNO3 | Enlace Dativo Carga Formal BACHILLERATO
Introducción a la estructura de Lewis del ácido nítrico
Resumen de la sección: En esta sección, el instructor introduce el tema de la estructura de Lewis del ácido nítrico y explica cómo determinar la carga formal de este compuesto.
Identificación de los elementos y su configuración electrónica
- El ácido nítrico está compuesto por hidrógeno, nitrógeno y oxígeno.
- La última capa de valencia del hidrógeno es 1s^1.
- La última capa de valencia del nitrógeno es 2s^2 2p^3.
- La última capa de valencia del oxígeno es 2s^2 2p^4.
Estructura de Lewis del ácido nítrico
- El nitrógeno se toma como el átomo central en la estructura de Lewis.
- Se colocan tres átomos de oxígeno alrededor del nitrógeno.
- Se añaden los átomos de hidrógeno junto a uno de los oxígenos.
Determinación de electrones en la última capa
- Cada átomo tiene una cantidad específica de electrones en su última capa:
- Hidrógeno: 1 electrón
- Nitrógeno: 5 electrones
- Oxígeno: 6 electrones
Dibujo y conteo final
- Se dibuja la estructura utilizando puntos para representar los electrones compartidos entre los átomos.
- Se cuentan todos los electrones presentes en la estructura, incluyendo los pares libres.
- En el caso del ácido nítrico, se obtienen 24 electrones en total.
Verificación de la regla del octeto
- Se verifica si cada átomo cumple con la regla del octeto, es decir, si tiene 8 electrones en su última capa o 2 para el hidrógeno.
- Se comprueba que todos los átomos en la estructura cumplen con esta regla.
Dibujo de la estructura de Lewis y verificación de la regla del octeto
Resumen de la sección: En esta sección, el instructor muestra cómo dibujar la estructura de Lewis utilizando enlaces sencillos y verifica nuevamente si cada átomo cumple con la regla del octeto.
Dibujo de enlaces sencillos
- Se dibujan los enlaces sencillos entre los átomos utilizando puntos para representar los electrones compartidos.
- Cada hidrógeno tiene un solo electrón compartido con un oxígeno.
- Cada oxígeno comparte dos electrones con el nitrógeno y dos electrones con otro oxígeno.
Verificación final de la regla del octeto
- Se verifica nuevamente si cada átomo cumple con la regla del octeto.
- Todos los átomos en el ácido nítrico cumplen con esta regla, ya que tienen 8 electrones en su última capa o 2 para el hidrógeno.
Conclusión sobre la estructura de Lewis del ácido nítrico
Resumen de la sección: En esta sección, el instructor concluye la explicación sobre la estructura de Lewis del ácido nítrico y destaca que todos los átomos en la estructura cumplen con la regla del octeto.
Cumplimiento de la regla del octeto
- Todos los átomos en el ácido nítrico cumplen con la regla del octeto, ya que tienen 8 electrones en su última capa o 2 para el hidrógeno.
- La estructura de Lewis muestra cómo se comparten los electrones entre los átomos para formar enlaces sencillos.
Fin de la explicación sobre la estructura de Lewis del ácido nítrico
Resumen de la sección: En esta sección final, el instructor concluye su explicación sobre la estructura de Lewis del ácido nítrico y destaca que todos los átomos en la estructura cumplen con la regla del octeto.
Formación de enlaces en el ácido nítrico
Resumen de la sección: En esta sección, se explica cómo se forman los enlaces en el ácido nítrico y se muestra la distribución de electrones en la estructura de Lewis.
Distribución de electrones y formación de doble enlace
- Se comparten dos electrones entre un oxígeno y un nitrógeno para formar un doble enlace.
- Se contabilizan los electrones previamente mencionados para asegurar que todos estén presentes.
Estructura de Lewis con doble enlace
- La estructura muestra los átomos de oxígeno, nitrógeno e hidrógeno conectados por enlaces.
- Se marcan los pares libres y los puntos representando los electrones compartidos.
Cumplimiento del octeto
- Se verifica si cada átomo cumple con la regla del octeto (8 electrones).
- El hidrógeno cumple con el octeto debido a sus 2 electrones compartidos.
- Los átomos de oxígeno cumplen con el octeto debido a sus 6 pares libres y 2 electrones compartidos.
- El nitrógeno no cumple con el octeto, ya que tiene 9 electrones.
Formación del enlace dativo
- Un electrón libre del oxígeno se une al nitrógeno para completar su octeto.
- El electrón libre del nitrógeno pasa a acompañar al electrón solitario del oxígeno.
- Esto forma un enlace dativo donde uno de los átomos dona sus electrones para formar el enlace.
Estructura de Lewis final
- Se muestra la estructura de Lewis del ácido nítrico con los enlaces y pares libres correctamente distribuidos.
- Todos los átomos cumplen con la regla del octeto.
Carga formal en el ácido nítrico
Resumen de la sección: En esta sección, se determina la carga formal de cada átomo en el ácido nítrico y se concluye que la molécula es neutra.
Determinación de la carga formal
- Se calcula la carga formal de cada átomo sumando los electrones compartidos y restando los pares libres.
- El hidrógeno tiene una carga formal neutra debido a sus 2 electrones compartidos.
- Los átomos de oxígeno tienen una carga formal neutra debido a sus 6 pares libres y 2 electrones compartidos.
- El nitrógeno tiene una carga formal negativa debido a sus 9 electrones (más del octeto).
Conclusión: Molécula neutra
- Dado que no hay cargas formales positivas o negativas en el ácido nítrico, se concluye que la molécula es neutra.
Cálculo de la carga formal del ácido nítrico
Resumen de la sección: En esta sección, se realiza el cálculo de la carga formal del ácido nítrico mediante el análisis de los electrones de valencia y los enlaces presentes en la molécula.
Cálculo de la carga formal del nitrógeno
- El número de electrones de valencia del nitrógeno es 5.
- Se cuentan los electrones no enlazados y se obtiene un total de 0.
- Se contabilizan los electrones enlazados, que son 2 por cada enlace, resultando en un total de 8.
- La fórmula para calcular la carga formal es: Electrones de valencia - Electrones no enlazados - 1/2 * Electrones enlazados.
- Aplicando la fórmula, se obtiene una carga formal para el nitrógeno igual a 1.
Cálculo de la carga formal del oxígeno
- El oxígeno forma un doble enlace con el nitrógeno.
- El número de electrones de valencia del oxígeno es 6.
- Se cuentan los electrones no enlazados y se obtiene un total de 4.
- Se contabilizan los electrones enlazados, que son 4 por el doble enlace.
- Aplicando la fórmula para calcular la carga formal, se obtiene una carga igual a -1.
Cálculo de la carga formal del hidrógeno
- El hidrógeno forma un enlace con el oxígeno.
- El número de electrones de valencia del hidrógeno es 1.
- No hay electrones no enlazados.
- Se contabilizan los electrones enlazados, que son 2 por el enlace.
- Aplicando la fórmula para calcular la carga formal, se obtiene una carga igual a 0.
Determinación de la carga formal total
- Se suman todas las cargas formales obtenidas para cada átomo en la molécula del ácido nítrico.
- La suma total de las cargas formales es igual a 0, lo que indica que la molécula es neutra.
Conclusión:
El cálculo de la carga formal del ácido nítrico muestra que la molécula es neutra. Este proceso permite determinar cómo se distribuyen las cargas eléctricas entre los átomos en una molécula y proporciona información sobre su estabilidad y propiedades químicas.