4 - Linfocitos T
Introducción a los Linfocitos T
Generación y Activación de Linfocitos T
- Se aborda la generación de linfocitos T, incluyendo los requisitos para su activación y la memoria inmunológica.
- El receptor para el antígeno de los linfocitos T (TCR) se forma durante la ontogenia mediante un proceso llamado recombinación somática.
- La estructura del TCR incluye cadenas alfa y beta, donde las porciones variables son más diversas que las porciones conservadas.
Estructura del Receptor TCR
- La porción variable de la cadena beta se genera a partir de fragmentos génicos llamados J y C, lo que permite una gran variabilidad en el receptor.
- En precursores de células T, estos fragmentos están en configuración germinal antes de ser seleccionados para formar el TCR.
Proceso de Recombinación Somática
- Durante la recombinación somática, se pierde material genético al seleccionar fragmentos específicos B1 y J, generando un rearreglo que da lugar a la cadena beta del TCR.
- La cadena alfa también se forma mediante un proceso similar con fragmentos B y J, contribuyendo a la diversidad del receptor.
Diversidad en Receptores Antigénicos
- Las enzimas recombinasas juegan un papel crucial al cortar y unir segmentos genéticos, aumentando así la diversidad antigénica.
- Este proceso permite generar múltiples receptores BCR diferentes entre sí debido a combinaciones aleatorias durante la recombinación.
Ontogenia y Migración de Linfocitos
- Una vez formada correctamente, la cadena abierta del TCR es expresada en superficie celular junto con una cadena alfa sustituta.
- Las células hijas resultantes continúan diversificando sus receptores mediante arreglos adicionales durante su desarrollo en el timo.
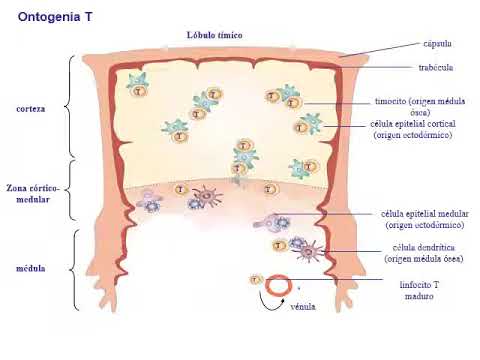
Ontogenia de los Linfocitos T
Proceso de Desarrollo en el Timo
- Los timocitos se enfrentan a un entorno compuesto principalmente por células del epitelio tímico cortical, diferente al de la médula tímica donde también hay células presentadoras de antígenos como macrófagos y células dendríticas.
- La clasificación de los timocitos se basa en la expresión de correceptores CD4 y CD8; aquellos que no expresan ninguno son llamados células Dulles negativas, mientras que los que expresan ambos son dobles positivas.
- Durante su desarrollo, los timocitos ingresan al timo como células dobles negativas y luego comienzan a expresar correceptores, transformándose en linfocitos T maduros simples positivos.
- En el estadio inicial, los timocitos son doble negativos (sin CD4 ni CD8), ubicados en la zona cortical con alta tasa de proliferación celular. Este estadio define el linaje de linfocitos T.
Rearreglo Genético y Expresión del Receptor
- Se inicia el rearreglo de las cadenas beta y J, crucial para la formación del receptor TCR. Este proceso involucra recombinasas y enzimas que aseguran un arreglo productivo.
- Una vez completado el rearreglo B-J, se transcribe y traduce la cadena beta junto con una cadena alfa sustituta; esto permite a los timocitos expresar por primera vez su receptor TCR.
- La expresión del receptor TCR genera señales que permiten a las células proliferar, aumentando así su número con material genético adecuado.
Selección Positiva y Muerte Celular
- Posteriormente ocurre un arreglo independiente para la cadena alfa; si este es exitoso, se expresa junto con la cadena beta en la membrana celular.
- La interacción entre los timocitos dobles positivos y las moléculas del complejo mayor de histocompatibilidad (MHC) es esencial para su supervivencia; sin esta interacción, las células mueren por abandono.
- El proceso conocido como selección tímica o inducción de tolerancia central es complejo e involucra múltiples mecanismos para asegurar que solo algunos timocitos sobrevivan tras interactuar adecuadamente con MHC.
Definición del Linaje Linfocitario
- Los timocitos deben reconocer moléculas MHC específicas para sobrevivir; aquellos que no lo logran sufren muerte celular programada.
- La selección positiva determina qué linfocito será funcional: si interactúa con MHC tipo 1 o tipo 2 definirá si será CD4 positivo o CD8 positivo respectivamente.
Mecanismos de Selección y Activación de Linfocitos T
Proceso de Selección en el Timo
- Las células del epitelio tímico medular muestran proteínas específicas, reguladas por factores de transcripción como el factor aire, que es crucial para la regulación genética en otros tejidos.
- Los timocitos que reciben señales intensas a través de su TCR son considerados peligrosos y autorreactivos, lo que lleva a su muerte en un proceso conocido como selección negativa.
- Para migrar desde la corteza hacia la médula, los timocitos deben ser seleccionados positivamente; esto implica superar la selección negativa sin recibir señales intensas.
- Los timocitos que sobreviven a este proceso se convierten en células T maduras capaces de reconocer las proteínas propias del organismo.
- No todas las proteínas propias entran en la zona medular; algunas células autorreactivas son controladas por mecanismos conocidos como inducción de tolerancia periférica.
Ontogenia y Activación de Linfocitos T
- Se discuten los mecanismos involucrados en la ontogenia de linfocitos T, destacando cómo estos superan procesos de selección positiva y negativa antes de emigrar del timo.
- Los linfocitos T vírgenes comienzan un tráfico por órganos linfáticos secundarios donde pueden ser activados por células dendríticas presentadoras de antígenos.
- La activación ocurre cuando los linfocitos T vírgenes interactúan con células dendríticas que presentan complejos peptídicos-MHC, facilitando así el reconocimiento específico del antígeno.
Interacción entre Linfocitos y Células Dendríticas
- Las células dendríticas inmaduras se activan mediante citoquinas proinflamatorias, lo cual incrementa su capacidad para procesar antígenos y expresar moléculas coestimuladoras necesarias para activar linfocitos T vírgenes.
- Estas células dendríticas se posicionan estratégicamente en áreas paracorticales dentro de los ganglios linfáticos gracias a quimiocinas específicas que guían su migración hacia estas zonas.
Señales Necesarias para Activación
- Los linfocitos T buscan sobre la superficie celular el complejo MHC-pepTido; si no lo encuentran, regresan a circulación para continuar buscando en otros órganos linfoides secundarios.
- La activación efectiva requiere dos señales: una señal primaria proveniente del reconocimiento del complejo péptido-MHC por parte del TCR y una segunda señal coestimuladora proporcionada por interacciones con CD28 y CD80/CD86 expresadas por las células dendríticas maduras.
- Tras recibir ambas señales adecuadamente, los linfocitos T producen IL-2 e inician su proliferación.
Receptores e Interacción Post-Aactivación
- Inicialmente, los linfocitos T vírgenes expresan receptores IL-2 de baja afinidad; tras activarse, pueden expresar receptores de alta afinidad al incluir cadenas alfa adicionales.
Activación y Proliferación de Linfocitos T
Interacción entre Linfocitos T y Células Dendríticas
- La alta afinidad provoca una expansión clonal de linfocitos T debido a la IL-2 que producen, recibiendo señales 1 y 2 para su activación.
- Los linfocitos T vírgenes reciben señales de activación de las células dendríticas, lo que lleva a la expresión de CD40L en los linfocitos T activados.
- La interacción entre CD40 en células dendríticas y CD40L en linfocitos T incrementa la capacidad coestimuladora de las células dendríticas.
Requerimientos Diferenciales para Activación
- Los linfocitos T CD8 vírgenes requieren un nivel más alto de moléculas coestimuladoras comparado con los CD4 para su correcta activación.
- La activación recíproca entre células dendríticas y linfocitos TCD4 es esencial para aumentar la capacidad coestimuladora necesaria para activar linfocitos TCD8.
Consecuencias de la Activación Inadecuada
- Si los linfocitos T vírgenes no reciben señal coestimuladora adecuada, se vuelven anérgicos, perdiendo capacidad de reactivarse y muriendo por apoptosis.
- Esta anergia permite que los linfocitos pasen directamente a órganos linfoides secundarios gracias a receptores específicos.
Migración y Acceso a Tejidos
- Los linfocitos vírgenes migran hacia órganos linfoides secundarios mediante quimiocinas y moléculas de adhesión específicas como L-selectina.
- Una vez activados, los patrones de expresión cambian, permitiendo el acceso a tejidos periféricos infectados.
Rol Específico de Células Dendríticas
- Las células dendríticas liberan sustancias específicas según el tejido del que derivan, influyendo en el perfil migratorio de los linfocitos efectores.
- Por ejemplo, las dendritas intestinales liberan ácido retinoico que promueve la expresión de moléculas adhesivas necesarias para acceder al intestino delgado.
Proceso Final: Activación Completa y Efectos Citotóxicos
- El proceso completo desde la activación hasta diferenciación en citotóxicos toma aproximadamente cinco días tras el encuentro con el antígeno.
Mecanismos de acción de los linfocitos T CD8 y NK
Funciones efectoras de los linfocitos T CD8
- Los linfocitos T CD8 pueden cumplir funciones efectoras al recibir la señal 1 de activación, lo que les permite reproducir citoquinas proinflamatorias y inducir apoptosis en células blanco.
- Existen dos mecanismos citotóxicos utilizados por los linfocitos T CD8: el mecanismo no secretorio, que involucra interacciones directas, y el mecanismo secretorio, que implica la liberación de perforinas y granzimas.
Comparación con células NK
- A diferencia de las células NK, donde el mecanismo se activa tras un balance positivo entre señales de activación e inhibición, los linfocitos T CD8 requieren reconocimiento específico del complejo antígeno-MHC para activar su respuesta citotóxica.
- El reconocimiento del complejo específico por parte del linfocito T CD8 induce la muerte celular en la célula blanco marcada.
Diferenciación de linfocitos T CD4 vírgenes
- Los linfocitos T CD4 vírgenes tienen una alta plasticidad en su perfil efector dependiendo del entorno citoquínico al momento de interactuar con células dendríticas.
- La diferenciación hacia perfiles efectores como Th1 o Th17 se ve influenciada por las citoquinas presentes durante el contacto inicial con las células presentadoras de antígenos.
Perfiles efectoras específicos
- Las células Th1 son cruciales para la inmunidad contra microorganismos intracelulares y virus; producen interferón gamma como principal citoquina.
- En presencia de IL-21 y alta afinidad del receptor TCR, los linfocitos TCD4 vírgenes pueden diferenciarse hacia un perfil Th folicular que activa a los linfocitos B.
Respuestas inmunitarias mediadas por diferentes perfiles
- El perfil Th2 se desarrolla en presencia de IL-4 y está asociado a respuestas frente a parásitos helmintos y enfermedades alérgicas; produce citoquinas como IL-4, IL-5 e IL-13.
- La diferenciación hacia el perfil Th17 ocurre bajo influencia de IL-16 y TGF-beta, siendo relevante en infecciones bacterianas y fúngicas.
Regulación inmune por perfiles específicos
- Las células reguladoras (Treg), producidas bajo condiciones específicas (IL10 y TGF-beta), juegan un papel importante en la regulación inmune.
- La elección del perfil efector durante la activación puede influir significativamente en respuestas antiinfecciosas o autoinmunitarias.
Interacción entre diferentes perfiles efectores
- En infecciones virales pueden coexistir respuestas Th1 junto con producción anticuerpos; esto es posible debido a las interacciones complejas entre diferentes tipos celulares.
- Ciertas citoquinas producidas por un tipo celular pueden inhibir la diferenciación hacia otros perfiles; por ejemplo, IL4 inhibe Th1/Th17 mientras que interferón gamma tiene efectos similares sobre Th2.
Factores de transcripción involucrados
- La iniciación en distintos perfiles efectores está regulada por factores de transcripción específicos que determinan tanto producción como características funcionales.
Mecanismos de Respuesta Inmunitaria
Activación de Macrófagos y Células NK
- Los macrófagos activados son cruciales en la respuesta inmune, donde el interferón gamma y la IL-2 inducen la activación de células NK y T CD8.
- La activación de macrófagos es esencial para combatir microorganismos intravesiculares, como las micobacterias que proliferan en vesículas intracelulares.
Tuberculosis y su Impacto Global
- Mycobacterium tuberculosis es el agente causante de la tuberculosis, propagándose a través del aire cuando personas infectadas tosen. Afecta principalmente los pulmones pero puede impactar otros órganos.
- Según un informe de la OMS (2019), la tuberculosis es una de las principales causas de mortalidad mundial, afectando a aproximadamente un cuarto de la población global.
Respuesta Inmunitaria ante Micobacterias
- Las micobacterias acceden a los alvéolos pulmonares, donde los macrófagos alveolares ingieren estos microorganismos, generando citoquinas proinflamatorias que reclutan más leucocitos.
- Los linfocitos Th1 específicos activan a los macrófagos para destruir bacilos internos, deteniendo así el crecimiento descontrolado y llevando a una infección latente.
Formación de Granulomas
- La formación de granulomas permite contener al patógeno sin erradicarlo completamente; participan tanto linfocitos Th1 como T CD8 citotóxicos en esta respuesta.
- Si se compromete el sistema inmunológico (por medicamentos o infecciones), el granuloma puede romperse, liberando bacilos hacia las vías aéreas y facilitando su diseminación.
Rol de Células Th17 y Th2
- Las células Th17 son importantes no solo en fenómenos autoinmunes sino también en la defensa contra infecciones por bacterias extracelulares y hongos.
- Los linfocitos T helper foliculares colaboran con linfocitos B vírgenes proporcionando señales necesarias para activar respuestas humorales efectivas.
Funciones Específicas de Células Th2
- Las células Th2 juegan un papel clave en respuestas inmunitarias frente a parásitos extracelulares e influyen en procesos alérgicos mediante producción de citoquinas como IL-4 e IL-5.
- Estas citoquinas favorecen cambios isotópicos en anticuerpos producidos por linfocitos B, promoviendo así una respuesta inmune efectiva contra parásitos.
Implicaciones Clínicas
- La producción de IL-13 por células Th2 ayuda en la reparación epitelial y secreción mucosa; además, promueve un subtipo específico de macrófago (M2).
Funciones de las Células T Regulatorias en la Inmunidad
Importancia de las Células T Regulatorias
- Las células T regulatorias (Treg) son cruciales para mantener la homeostasis y tolerancia inmunológica, limitando la actividad de clones autorreactivos en los tejidos periféricos.
- Existen dos tipos principales: las naturales (CD4+ Foxp3+) que emigran del timo, y las inducibles que se desarrollan en respuesta a antígenos en órganos linfáticos secundarios.
Generación de Memoria Inmunológica
- La memoria inmunológica se genera tras una primoinfección, donde se inicia una respuesta inmune innata seguida por una adaptativa.
- En un segundo encuentro con el mismo patógeno, la respuesta es más rápida y eficiente gracias a la generación previa de células T efectoras.
Dinámica de Respuesta Inmunitaria
- Durante el primer desafío con un antígeno, se produce una contracción del pool efector y se generan células T de memoria que son más numerosas que los linfocitos vírgenes iniciales.
- Con sucesivos encuentros con el mismo antígeno, aumenta la cantidad de células T de memoria disponibles para responder rápidamente.
Activación y Proliferación
- Las células T de memoria pueden activarse y proliferar en ausencia del antígeno mediante citoquinas proinflamatorias como IL-12 e interferones tipo I.
- Esta activación permite que las células T permanezcan funcionales incluso sin presencia continua del patógeno.
Tipos de Células T de Memoria
- Se identifican dos grandes grupos: las células T de memoria centrales (que tienen características similares a los linfocitos vírgenes) y las efectores (que no expresan L-selectina).
- Las células T efectoras residentes pueden formar poblaciones estables en tejidos específicos, actuando como centinelas ante reinfecciones.
Respuesta Frente a Reinfectados
- En individuos previamente infectados, las células T de memoria pueden alojarse en tejidos y actuar rápidamente ante reingresos del patógeno.